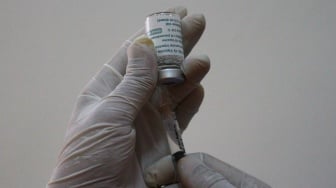
Penny melanjutkan, Organisasi Kesehatan Dunia (WHO) dan sejumlah regulator obat dunia mensyaratkan penerbitan EUA harus mengacu pada laporan utuh dari uji klinis tahap pertama dan kedua, kemudian data pemantauan selama enam bulan setelah penyuntikan vaksin dosis yang terakhir.
Selain itu, EUA juga harus mengacu pada data analisis tiga bulan observasi dari uji klinis tahap ketiga, serta data efikasi minimum 50 persen.
Penny menuturkan data tersebut tidak mungkin didapat pada pekan ketiga Desember 2020 dari uji klinis fase ketiga vaksin Sinovac di Bandung.
"Kami sudah menyampaikan ke presiden dan menteri kesehatan bahwa data tidak bisa didapatkan untuk minggu ketiga Desember 2020 ini," kata Penny dalam Rapat Kerja Komisi IX DPR RI pada Selasa (17/11/2020).
Menurut Penny, BPOM juga telah mencoba meminta data hasil uji klinis tahap ketiga vaksin yang sama kepada Brasil.
Brasil telah memulai uji klinis lebih dulu dari Indonesia dan datanya dapat digunakan sebagai salah satu rujukan penerbitan EUA.
"Kami sudah dapat info dari Brasil bahwa mereka tidak bisa memberikan, Sinovac juga tidak bisa memberikan sehingga datanya tidak lengkap," kata dia.
"Berdasarkan standar yang ada, tentu tidak mungkin kami bisa berikan EUA pada minggu ketiga Desember 2020," ujar Penny.
Baca Juga: Pemerintah Lakukan Simulasi Vaksinasi Covid-19, Untuk Apa?