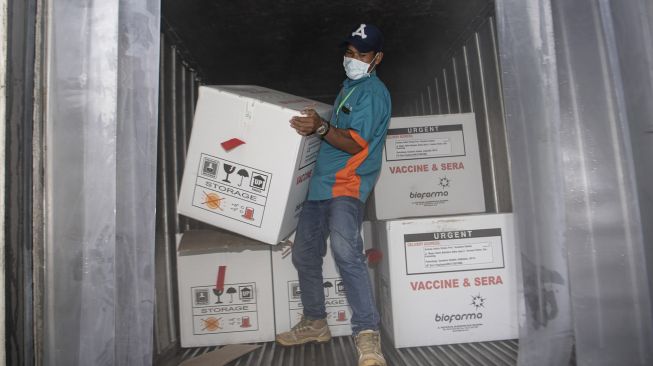
Suara.com - Badan Pengawasan Obat dan Makanan (BPOM) telah menerbitkan sertifikat lot release pada 1,2 dosis vaksin Covid-19 Sinovac yang tiba 6 Desember 2020 lalu.
Selanjutnya, BPOM akan segera menerbitkan juga sertifikat lot release untuk 1,8 juta vaksin yang datang pada 31 Desember 2020.
Juru Bicara Vaksinasi Covid-19 Lucia Rizka Andalusia mengatakan, BPOM juga tengah melakukan sampling dan pengujian vaksin saat kedatangan vaksin di Bandara Soekarno Hatta.
"Pada proses penerimaan di bandara, Badan POM melakukan pengecekan kesesuaian dokumen, serta kesesuaian suhu tempat penyimpanan vaksin coronavac," kata Lucia dalam keterangan pers perkembangan vaksinasi di Istana Kepresidenan Jakarta, Senin (4/1/2021).
Sertifikat Lot release merupakan persyaratan penting yang harus dipenuhi dalam memastikan kualitas vaksin.
Syarat itu termasuk standar yang ditetapkan World Health Organization (WHO), yaitu berupa proses evaluasi yang dilakukan otoritas obat di setiap negara untuk menjamin mutu setiap lot atau setiap batch vaksin tersebut.
"Untuk penerbitan sertifikat ini, Badan POM melakukan pengujian di laboratorium Pusat Pengembangan Pengujian Obat dan Makanan Nasional," kata Lucia.
Sementara untuk proses percepatan penerbitan izin penggunaan darurat atau EUA vaksin Covid-19, BPOM melakukan rolling submission, di mana data yang dimiliki oleh industri farmasi dapat disampaikan secara bertahap.
Lucia melanjutkan, evaluasi terhadap data uji praklinik, uji klinik fase 1 dan fase 2 untuk menilai keamanan dan respon imun dari penggunaan vaksin juga telah dilakukan BPOM. Termasuk hasil uji klinik fase 3 yang dipantau dalam periode 1 bulan setelah suntikan yang kedua.
Baca Juga: Hingga Kini, Unpad Sudah Uji Klinis Lebih dari 30 Vaksin
"Tentunya, sesuai persyaratan dari WHO, minimal pengamatan harus dilakukan sampai 3 bulan untuk interim analisis. Yang akan digunakan untuk mendapatkan data keamanan dan khasiat vaksin sebagai data dukung pemberian EUA," tegasnya.