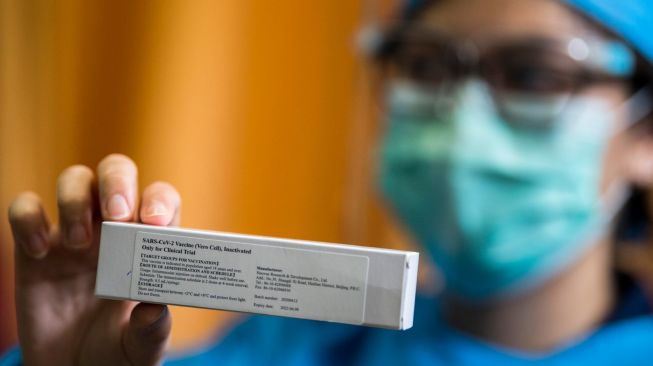
Suara.com - Plt Deputi Bidang Pengawasan Obat, Narkotika, Psikotropika, Prekursor, dan Zat Adiktif Badan Pengawas Obat dan Makanan (BPOM), Dra Togi J Hutadjulu Apt MHA, memastikan pihaknya akan sangat berhati-hati terkait rencana vaksinasi Covid-19.
“BPOM mengedepankan kepentingan kesehatan masyarakat. Jadi, kami perketat untuk mengambil langkah-langkah strategis pengawalan penyediaan vaksin Covid-19 ini,” ujar Togi dalam pernyataannya seperti dikutip dari laman Satgas Covid-19, Selasa (3/11/2020).
Lebih lanjut, kata dia bahwa pihaknya memiliki standar dalam pemberian izin penggunaan vaksin, yakni melalui proses uji klinik. Produk juga harus dijamin melalui evaluasi persyaratan mutu yang sesuai dengan Cara Pembuatan Obat yang Baik (CPOB).
Setelah proses evaluasi tersebut dilalui dan vaksin dianggap memenuhi syarat dari aspek keamanan, khasiat, dan mutu, barulah Badan POM dapat memberikan perizinan penggunaan. Perizinan penggunaan tersebut dapat berupa Emergency Use Authorization (EUA) atau izin edar.
Baca Juga: Pemilu Berpotensi Jadi Klaster Baru Corona, KPU Pandeglang Lakukan Hal Ini
![Ilustrasi vaksin Covid-19. [Pearson0612/Pixabay]](https://media.suara.com/pictures/653x366/2020/10/14/12458-vaksin-covid-19.jpg)
EUA sendiri merupakan suatu mekanisme registrasi khusus untuk obat dan vaksin pada kondisi darurat seperti pandemi COVID-19 saat ini, dengan mengacu pada pedoman yang sudah ditetapkan Organisasi Kesehatan Dunia (WHO).
Berdasarkan ketentuan tersebut, industri farmasi yang diberikan EUA bertanggung jawab terhadap mutu vaksin, mulai dari bahan baku, pembuatan, pelulusan batch vaksin, hingga peredaran dan penggunaan pada pasien.
“Untuk mendapatkan izin edar, tentunya diperlukan data uji klinik yang lebih luas dan waktu panjang. Pengambilan keputusan pemberian persetujuan penggunaan darurat ini harus dilakukan dengan pertimbangan kemanfaatan yang lebih tinggi dari pada risikonya,” jelasnya.
Selain itu, BPOM juga akan mengawasi rantai pendistribusian vaksin Covid-19 di Indonesia. Hal ini berkaitan dengan penyimpanan khusus pada temperatur 2–8 derajat celcius. Manajemen rantai dingin ini merupakan hal yang krusial untuk menjaga mutu vaksin sampai ke pengguna.
“Setelah proses pemberian vaksin dilaksanakan, kami terus melakukan pengawasan untuk aspek keamanan melalui program kegiatan pemantauan efek samping atau yang dikenal dengan farmakovigilans,” beber Togi.
Baca Juga: Kecamatan Cinere dan Cimanggis di Depok Masuk Zona Kuning
Dia juga menerangkan apabila terdapat peningkatan frekuensi efek samping, BPOM berhak meninjau kembali aspek khasiat dan keamanan vaksin tersebut. Hasil pemantauan ini dikaji bersama para klinisi dan ahli di bidangnya.
“Jika ditemukan bahwa risiko menjadi lebih besar dari pada manfaatnya,tentu ini akan ditindaklanjuti dengan melakukan komunikasi sejumlah pihak. Kalau memang ditemukan adanya risiko keamanan yang tinggi, kami pastikan akan cabut EUA tersebut,” tuturnya.
Adapun, rencananya pemberian vaksinasi ini berlangsung pada akhir 2020 mendatang. Nantinya vaksin ini menggunakan vaksin Covid-19 buatan AstraZeneca dari Inggris dan Sinopharm dari China, yang sudah dibeli negara hingga jutaan dosis.